মৌলিক পদার্থের যে ক্ষুদ্রতম কণার মধ্যে মৌলটির সমস্ত ধর্ম উপস্থিত থাকে এবং যা রাসয়ানিক বিক্রিয়ায় অংশগ্রহণ করে তাকে মৌলিক পদার্থটির পরমাণু বলে। সমস্ত কঠিন, তরল, গ্যাস এবং আয়ন -এর গঠনের মূলে রয়েছে নিস্তরিত বা আধানগ্রস্ত পরমাণু। পরমাণুর আকার খুবই ক্ষুদ্র; সাধারনত এরা দৈর্ঘ্যে ১০০ পিকোমিটার (১ মিটারের ১০,০০০,০০০,০০০ ভাগের ১ ভাগ)।
পরমাণুর মাত্রা এই ক্ষুদ্রাকার হওয়ার কারণেই এর আচরনের বৈশিষ্টতা প্রথাগত পদার্থবিদ্যার সূত্র দিয়ে ব্যাখ্যা করা যায় না।
# বহুনির্বাচনী প্রশ্ন
মৌলিক কণিকা (Fundamental Particles)
যে সব সূক্ষ্ম কণিকা দ্বারা পরমাণু গঠিত, তাদেরকে মৌলিক কণিকা বলে। পরমাণুতে তিন ধরনের মৌলিক কণিকা থাকে। যথা- ইলেকট্রন, প্রোটন এবং নিউট্রন।
| ইলেকট্রন | পরমাণুর ক্ষুদ্রতম কণিকা ইলেকট্রন |  |
| প্রকৃত ভর । প্রতীক e- | ||
| চার্জ বা আধান: ঋণাত্মক ( কুলম্ব) | ||
| প্রোটন | একটি হাইড্রোজেন পরমাণু থেকে একটি ইলেকট্রন সরিয়ে নিয়ে যা থাকে তা একটি প্রোটন। এই কারণে প্রোটনের সংকেত । |  |
| প্রকৃত ভর ।প্রতীক P | ||
| চার্জ বা আধান: ধনাত্মক (কুলম্ব) | ||
| নিউট্রন | নিউট্রনের কোনো আধান নাই। Neutral হওয়ার কারণেই এর এই নামকরণ করা হয়েছে। |  |
| প্রকৃত ভর । প্রতীক n |
# বহুনির্বাচনী প্রশ্ন
পরমাণুর গঠন (Structure of Atoms)
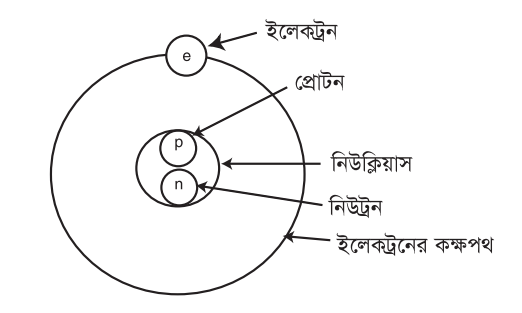
পরমাণুর একটি কেন্দ্র আছে, যার নাম নিউক্লিয়াস (Necleus)। এই নিউক্লিয়াসে প্রোটন ও নিউট্রন অবস্থান করে। সুতরাং পরমাণুর সকল ধনাত্মক আধান এবং প্রায় সম্পূর্ণ ভরই নিউক্লিয়াসে কেন্দ্রীভূত। ইলেকট্রন নিউক্লিয়াসের বাহিরে থাকে এবং তার চারদিকে ভ্রমণ করে। পরমাণু বৈদ্যুতিক নিরপেক্ষ, কারণ একটি পরমাণুতে যতটি প্রোটন আছে, ততটি ইলকট্রনও আছে। অবশ্য পরমাণু হতে সহজেই ইলেকট্রন বের করে আনা যায় এবং বাহির হতে অতিরিক্ত ইলেকট্রন যোগও করা যায়। তখন আর বিদ্যুৎ নিরপেক্ষ পরমাণু থাকে না, আধানযুক্ত আয়নের সৃষ্টি হয়। ঘর্ষণ, তাপ, রাসায়নিক প্রভৃতি প্রক্রিয়ায় সহজেই পরমাণু থেকে ইলেকট্রন নির্গত হয়।
# বহুনির্বাচনী প্রশ্ন
পরমাণুর ইলেকট্রন বিন্যাস (Electronic configuration of atoms)
পরমাণুতে ইলেকট্রনগুলো যেভাবে সজ্জিত বা বিন্যস্ত থাকে তাই ঐ পরমাণুর ইলেকট্রন বিন্যাস। পরমাণুর প্রতিটি শক্তিস্তরে সর্বোচ্চ ইলেকট্রনের সংখ্যা 2n2।
প্রথম শক্তিস্তরে (n=1) সর্বোচ্চ ইলেকট্রন ধারণক্ষমতা =2n2 = 212 = 2 .
দ্বিতীয় শেলে সর্বোচ্চ ইলেকট্রন ধারণক্ষমতা = 2n = 2 22 = 8
তৃতীয় শেলে সর্বোচ্চ ইলেকট্রন ধারণক্ষমতা = 2n = 2 32 = 18
চতুর্থ শেলে সর্বোচ্চ ইলেকট্রন ধারণক্ষমতা = 2n = 2 42 = 32

# বহুনির্বাচনী প্রশ্ন
পারমাণবিক সংখ্যা (Atomic Number)
নিউক্লিয়াসে অবস্থিত প্রোটনের সংখ্যাকে মৌলের পারমাণবিক সংখ্যা বলা হয়। একে Z দ্বারা প্রকাশ করা হয়। যে কোনো মৌলের স্বাতন্ত্র্য এই সংখ্যার উপর নির্ভর করে। এটি যে কোনো মৌলের মৌলিক ধর্ম। যেমন- কার্বনের পরমাণুতে ৬টি প্রোটন আছে। সুতরাং কার্বনের পারমাণবিক সংখ্যা ৬।
# বহুনির্বাচনী প্রশ্ন
ভর সংখ্যা বা নিউক্লিয়ন সংখ্যা (Mass Number)
নিউক্লিয়াসে অবস্থিত প্রোটন ও নিউট্রনের মোট সংখ্যাকে একটি পরমাণুর ভর সংখ্যা বলা হয়। ভর সংখ্যাকে A দ্বারা প্রকাশ করা হয়। কোনো পরমাণুর অন্তর্গত প্রোটন ও নিউট্রনের মোট সংখ্যাকে ভর সংখ্যা বলা হয়। ভর সংখ্যা A, প্রোটন সংখ্যা P এবং নিউট্রন সংখ্যা N হলে, পরমাণুর ভর সংখ্যা A = P + N। সোডিয়ামের একটি পরমাণুতে প্রোটন আছে ১১টি, নিউট্রন আছে ১২টি। সুতরাং সোডিয়ামের এই পরমাণুর ভর সংখ্যা ২৩।
কতিপয় গুরুত্বপূর্ণ মৌলের পারমাণবিক সংখ্যা ও ভর সংখ্যা
মৌল | পারমাণবিক সংখ্যা | ভর সংখ্যা | মৌল | পারমাণবিক সংখ্যা | ভর সংখ্যা |
| হাইড্রোজেন | ১ | ১ | সিলিকন | ১৪ | ২৮ |
| হিলিয়াম | ২ | ৪ | ক্যালসিয়াম | ২০ | ৪০.০৮ |
| কার্বন | ৬ | ১২ | আর্সেনিক | ৩৩ | ৭৫ |
| সোডিয়াম | ১১ | ২৩ | পারদ | ৮০ | ২০০.৬ |
| ম্যাগনেসিয়াম | ১২ | ২৪ | ইউরেনিয়াম | ৯২ | ২৩৮ |
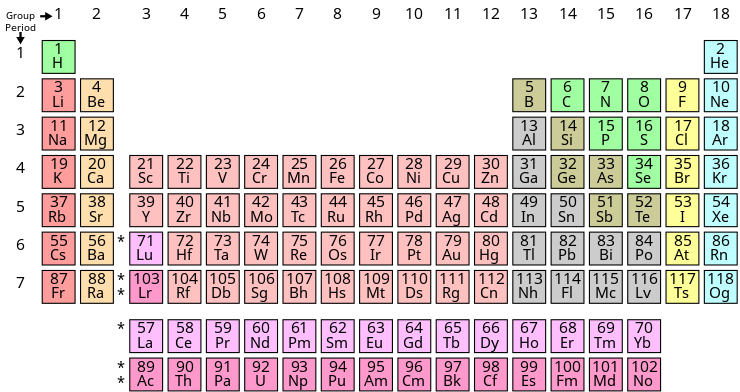
পর্যায় সারণীর জনক মেন্ডেলিফ। মেন্ডেলিফের পর্যায় সারণীর ভিত্তি ছিল পারমাণবিক ভর। আধুনিক পর্যায় সারণীর ভিত্তি পারমাণবিক সংখ্যা। আধুনিক পর্যায় সারণীতে ৭ টি পর্যায় পর্যায় এবং ৯টি গ্রুপ রয়েছে।
ক্ষার ধাতু (Alkali metal)
যে সকল ধাতু পানির সঙ্গে সরাসরি বিক্রিয়া করে তীব্র ক্ষার গঠন করে, তাকে ক্ষার ধাতু বলে। ক্ষার ধাতুগুলোর নাম লিথিয়াম, সোডিয়াম, পটাসিয়াম, রুবিডিয়াম এবং সিজিয়াম। পর্যায় সারণিতে ক্ষার ধাতুগুলোর অবস্থান IA গ্রুপে।
মৃৎক্ষার ধাতু (Mrtksara metal)
যে সকল ধাতু ভূ-ত্বকের মৃত্তিকার উপাদানরূপে পাওয়া যায় এবং পানির সঙ্গে বিক্রিয়া করে ক্ষারক গঠন করে, তাকে মৃৎক্ষার ধাতু বলে। উদাহরণ: ক্যালসিয়াম, ম্যাগনেসিয়াম। পর্যায় সারণিতে মৃৎক্ষার ধাতুগুলোর অবস্থান IIA গ্রুপে।
নিষ্ক্রিয় গ্যাস (Noble gas)
পর্যায় সারণির শূন্য গ্রুপের মৌলসমূহ রাসায়নিকভাবে নিষ্ক্রিয় এবং কক্ষ তাপমাত্রায় গ্যাসীয়। এদের নিষ্ক্রিয় গ্যাস বলে। নিষ্ক্রিয় গ্যাস ৬টি, যথা- হিলিয়াম (He), নিয়ন (Ne), আর্গন (Ar), ক্রিপ্টন (Kr), জেনন (Xe) এবং রেডন (Rn)। নিষ্ক্রিয় গ্যাসসমূহের সর্ববহিঃস্থ স্তরে ৮টি ইলেকট্রন থাকে (ব্যতিক্রম: হিলিয়াম)।
হিলিয়ামের সর্ববহিঃস্থ স্তরে ২টি ইলেকট্রন থাকে। মৌলিক গ্যাস' (হাইড্রোজেন (H2), অক্সিজেন (O2)] এর অণুসমূহ দ্বিপরমাণুক। কিন্তু নিষ্ক্রিয় গ্যাসের অণুসমূহ এক পরমাণুক। যেমন: হিলিয়াম (He), নিয়ন (Ne)। মৌলিক গ্যাস র্যাডন সর্বাপেক্ষা ভারি। রেডন তেজস্ক্রিয় মৌল। বিজ্ঞানী ডর্ন ১৯০০ সালে রেডিয়ামের তেজস্ক্রিয় বিভাজন হতে রেডন আবিষ্কার করেন। সূর্যে মৌলিক পদার্থের মধ্যে হিলিয়াম (He) এর পরিমাণ সবচেয়ে বেশি।
ব্যবহার
- বেলুনে এবং ডুবুরিদের জন্য হাইড্রোজেনের পরিবর্তে হিলিয়াম ব্যবহার করা। হাইড্রোজেন হিলিয়াম অপেক্ষা হালকা হলেও হাইড্রোজেন দাহ্য পক্ষান্তরে হিলিয়াম নিষ্ক্রিয়।
- সাধারণ বৈদ্যুতিক বাল্বের ভিতরে সাধারণত নাইট্রোজেন গ্যাস ব্যবহার করা হয়। কিন্তু টিউব লাইটে সাধারণত নিয়ন, আর্গন প্রভৃতি গ্যাস ব্যবহৃত হয়।
- ফটোগ্রাফিক ফ্লাশ লাইটে জেনন গ্যাস ব্যবহৃত হয়।
আইসোটোপ
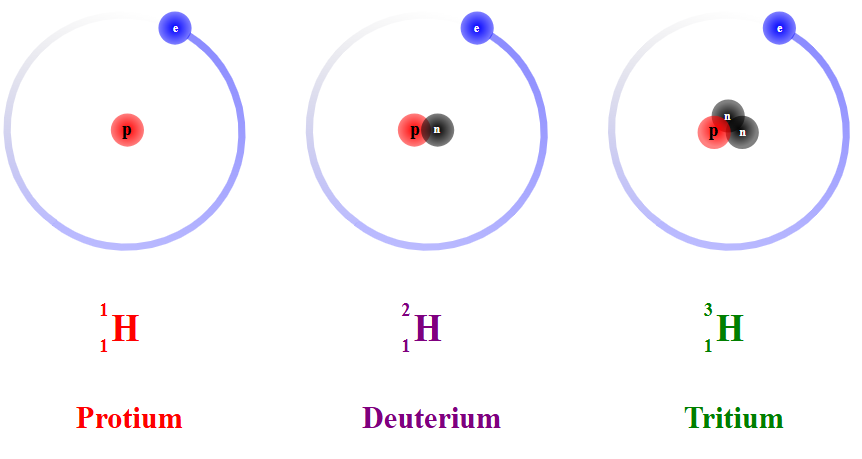
যে সকল পরমাণুর পারমাণবিক সংখ্যা সমান কিন্তু ভর সংখ্যা ভিন্ন, তাদেরকে পরস্পরের আইসোটোপ বলা হয়। অন্যভাবে বলা যায়, এটমিক সংখ্যা একই হওয়া সত্ত্বেও নিউক্লিয়াসের নিউট্রন সংখ্যা বেশি হওয়ার ফলে ভরসংখ্যা বেড়ে যায়, তাদেরকে পরস্পরের আইসোটোপ বলা হয়। যেমন: হাইড্রোজেনের আইসোটোপগুলো হলো প্রোটিয়াম (1H1), ডিউটেরিয়াম (2H1) ও ট্রিটিয়াম (3H1)। হাইড্রোজেন, ডিউটেরিয়াম এবং ট্রিটিয়াম তিনটিরই পারমাণবিক সংখ্যা 1 কিন্তু ভর সংখ্যা যথাক্রমে 1, 2 এবং 3। লক্ষণীয়, হাইড্রোজেন পরমাণুতে কোনো নিউট্রন থাকে না। ইউরেনিয়ামের তিনটি আইসোটোপ (234U92), (235U92), (238U92) । পারমাণবিক চুল্লীতে বহুল ব্যবহৃত আইসোটোপ (235U92)|
# বহুনির্বাচনী প্রশ্ন
50%
99.3%
0%
69.3%
60Co
32p
65Zn
131 I
আইসোটোন (Isotone)
যে সকল পরমাণুর নিউট্রন সংখ্যা সমান কিন্তু প্রোটন সংখ্যা ও ভর সংখ্যা ভিন্ন, তাদেরকে পরস্পরের আইসোটোন বলে। যেমন: সিলিকন (30Si14), ফসফরাস (31P15) এবং সালফার (32S16) পরস্পরের
আইসোটোন কারণ
সিলিকনের নিউট্রন সংখ্যা = 30 - 14 = 16
ফসফরাসের নিউট্রন সংখ্যা = 31 - 15 = 16
সালফারের নিউট্রন সংখ্যা = 32 - 16 = 16
কিন্তু এ সকল মৌলের প্রোটন সংখ্যা এবং ভর সংখ্যা ভিন্ন।
# বহুনির্বাচনী প্রশ্ন
আইসোটোপ
আইসোটোন
আইসোবার
আইসোমার
যে সকল পরমাণুর ভর সংখ্যা সমান কিন্তু প্রোটন সংখ্যা ভিন্ন, তাদেরকে পরস্পরের আইসোবার বলা হয়। যেমন: কপার (64Cu29) এবং জিংক (64Zn30) পরস্পরের আইসোবার কারণ উভয়ের ভরসংখ্যা 64 কিন্তু প্রোটন সংখ্যা যথাক্রমে 29 এবং 30।
Read more






